Metanas
| |
Šiam straipsniui ar jo daliai trūksta išnašų į patikimus šaltinius. Jūs galite padėti Vikipedijai pridėdami tinkamas išnašas su šaltiniais. |
| Metanas | |
|---|---|
| |
| Sisteminis (IUPAC) pavadinimas | |
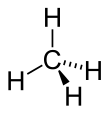
| Metanas | |
| CAS numeris | [74-82-8] |
| InChI | 1/CH4/h1H4 |
| Cheminė formulė | CH4 |
| Molinė masė | 16,0425 g/mol |
| SMILES | C |
| Rūgštingumas (pKa) | |
| Bazingumas (pKb) | |
| Valentingumas | |
| Fizinė informacija | |
| Tankis | |
| Išvaizda | Bespalvės dujos |
| Lydymosi t° | -182,5 °C, 91 K, |
| Virimo t° | -161,6 °C, 112 K, |
| Lūžio rodiklis (nD) | |
| Klampumas | |
| Tirpumas H2O | 3,5 mg/100 mL (17 °C) |
| Šiluminis laidumas | |
| log P | |
| Garavimo slėgis | |
| kH | |
| Kritinis santykinis drėgnumas | |
| Farmakokinetinė informacija | |
| Biotinkamumas | |
| Metabolizmas | |
| Pusamžis | |
| Pavojus | |
| MSDS | |
| ES klasifikacija | Ypač degios (F+) |
| NFPA 704 | |
| Žybsnio t° | -188 °C |
| Užsiliepsnojimo t° | |
| R-frazės | R12 |
| S-frazės | (S2), S9, S16, S33 |
| LD50 | |
| Struktūra | |
| Kristalinė struktūra | |
| Molekulinė forma | |
| Dipolio momentas | |
| Simetrijos grupė | |
| Termochemija | |
| ΔfH |
|
| Giminingi junginiai | |
| Giminingi alkanai | Etanas, Propanas |
| Giminingi junginiai | Metanolis, Chlorometanas |
| Giminingos grupės | |
- Apie Argentinos miestą žiūrėkite: San Chose de Metanas
Metanas – pats paprasčiausias alkanų atstovas, kurio molekulės formulė: CH4. Tai pagrindinė gamtinių dujų sudedamoji dalis. Sudegus vienai molekulei metano, susidaro viena molekulė CO2 (anglies dioksido) ir dvi molekulės H2O (vandens):
CH4 + 2O2 → CO2 + 2H2O.
Kadangi metanas yra labai paplitęs ir labai degus, jis plačiai naudojamas kaip kuras.
Žemės plutoje slypi dideli metano kiekiai. Taip pat nemaža metano dalis susidaro pūvant be oro augalų ir gyvūnų liekanoms.
